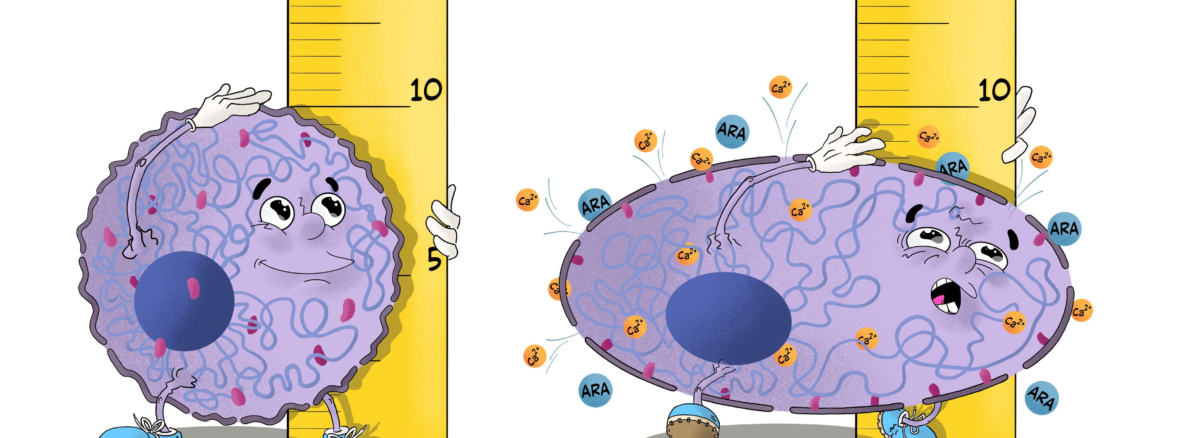
Die Verformung des Zellkerns löst eine Signalkaskade für das Entkommen von Krebszellen aus. Grafik: Wojciech Garncarz (St. Anna Kinderkrebsforschung)
Wie Krebszellen aus Tumoren flüchten
Körperzellen versuchen zu entkommen, wenn sie in dichtem Gedränge vieler Zellen „eingekesselt“ werden. Ein Wissenschaftler der St. Anna Kinderkrebsforschung hat gemeinsam mit Kolleginnen und Kollegen entdeckt, dass der Zellkern eine Art »Fluchtreflex« auslöst, um die Zelle zu befreien. Dieser Reflex wird aktiviert, sobald der von außen ausgeübte Druck den Zellkern zu sehr komprimiert. Diese neue Erkenntnis könnte dazu beitragen, die metastatische Ausbreitung von Tumoren und das Ansprechen auf die Behandlung vorherzusagen. Diese neuen Forschungsergebnisse wurden im weltweit renommierten Fachjournal Science veröffentlicht.
Wie der Mensch, so schützen auch die Zellen im menschlichen Körper ihren persönlichen Raum. Sie scheinen zu wissen, wie viel Platz sie brauchen. Wird es zu eng, versuchen die meisten Zellen, sich mehr Raum zu verschaffen. An dem Mechanismus, der es Zellen ermöglicht dichtem Gedränge zu entgehen, dürfte ein bisher unerkannter Akteur beteiligt sein – der Zellkern. Das haben Forscherinnen und Forscher der St. Anna Kinderkrebsforschung Wien, des King’s College London, des Institute Curie Paris und der ETH Zürich Basel in ihrer aktuellen Arbeit gezeigt.
Der menschliche Körper besteht aus Billionen von Zellen, die in begrenztem Raum wachsen, was häufig zu einer Zellverdichtung führt…

Diese Verdichtung spitzt sich zu, wenn Zellwachstum und ‑proliferation während der Tumorbildung außer Kontrolle geraten. Dadurch sind die beteiligten Zellen Druckbelastungen aus ihrer Mikroumgebung ausgesetzt. Aber wie kommen Tumorzellen mit dem Platzmangel und den Druckbelastungen zurecht? Bei der Beantwortung dieser Frage stellten die Forscherinnen und Forscher fest, dass Zellen in der Lage sind, die Kompression der Umgebung wahrzunehmen.
Um das zu bewerkstelligen nutzen Zellen ihre größte und rigideste Untereinheit, den Zellkern. Wenn Zellen so stark zusammengedrückt werden, dass der Kern physisch deformiert wird, entfalten sich die Kernmembranen und dehnen sich aus. Diese Veränderungen werden von spezialisierten Proteinen erkannt und aktivieren die zelluläre Kontraktion. Diese Fähigkeit, kontraktile Kräfte zu entwickeln, hilft der Zelle, sich in einem »Fluchtreflex«-Mechanismus aus ihrer komprimierenden Mikroumgebung herauszudrücken. Daher schlussfolgert das Forscherteam, dass der Zellkern als Messregler fungiert (siehe Abbildung). Er ermöglicht es lebenden Zellen, ihren persönlichen Raum zu messen und spezifische Reaktionen auszulösen, sobald ihr persönlicher Raum über ein bestimmtes Maß eingeschränkt wird.
Fettarme Kost, um Schwächen im Krebs-Stoffwechsel anzugreifen?
Wie die Wissenschaftlerinnen und Wissenschaftler in der Arbeit beschreiben, ist die Ca2+-abhängige Phospholipase cPLA2 ein Protein, das die Dehnung der Kernmembran bei Kompression der Zelle wahrnimmt. Erstautor Dr. Alexis Lomakin betont, dass cPLA2 ein mit Medikamenten angreifbares Ziel darstellt. »Pharmazeutische Unternehmen testen derzeit niedermolekulare Inhibitoren von cPLA2. Basierend auf unseren Daten könnte die Herunterregulierung der cPLA2-Aktivität in Tumorzellen deren Fähigkeit beeinträchtigen, dem Primärtumor zu entkommen und an entfernte Stellen zu metastasieren«, erklärt Lomakin.
cPLA2-Inhibitoren verhindern die Produktion von Arachidonsäure (ARA), was sich in der Folge auf die Zellwanderung, das Wachstum und das Überleben der Zellen auswirkt. Zellen können ARA jedoch auch aus ihrer Umgebung gewinnen. Die westliche Ernährung ist zum Beispiel eine potente Quelle für Omega-6-Fettsäuren wie ARA. Die Einschränkung der Fettzufuhr über die Nahrung und die Aufnahme von Omega-3- anstelle von Omega-6-Fettsäuren könnte mit cPLA2-Inhibitoren synergistisch wirken, um das Entkommen von Tumorzellen aus überfüllten Gebieten einzuschränken. »Die Prüfung dieser Hypothese ist eine sehr spannende Aufgabe in unserer zukünftigen Forschung«, resümiert Lomakin.
Potenzieller prädiktiver Marker für Chemo-Resistenz
Überraschend war es, den Zellkern als einen aktiven Akteur zu identifizieren, der mechanische Einflüsse von außen schnell in biochemische Signale oder Stoffwechselleistungen übersetzt. Bisher wurde der Zellkern als passiver Speicher für genetisches Material betrachtet. »Wir sind sehr gespannt, was als nächstes kommt«, sagt. Lomakin. Seiner Meinung nach könnte die Messung starker Kerndeformationen das Metastasierungspotenzial und die Resistenz gegen Chemo- und Immuntherapie vorhersagen.
»Über viele Jahre hinweg haben Pathologinnen und Pathologen die Veränderungen der Zellkernform untersucht, um zwischen verschiedenen Stadien des Tumorwachstums zu unterscheiden. Wie sich die strukturell-mechanischen Veränderungen des Zellkerns funktionell auf Krebszellen auswirken, blieb jedoch völlig unerforscht«, sagt Lomakin.
Publikation
The nucleus acts as a ruler tailoring cell responses to spatial constraints
A. J. Lomakin*†‡, C. J. Cattin†, D. Cuvelier, Z. Alraies, M. Molina, G. P.
F. Nader, N. Srivastava, P. J. Saez, J. M. Garcia-Arcos, I. Y. Zhitnyak,A. Bhargava,
M. K. Driscoll, E. S. Welf, R. Fiolka, R. J. Petrie, N. S. De Silva, J. M. González-Granado, N. Manel, A. M. Lennon-Duménil, D. J. Müller*, M. Piel*‡
*Corresponding authors.
†These authors contributed equally to this work.
‡These authors contributed equally to this work.
Science, October 16, 2020
https://science.sciencemag.org/content/370/6514/eaba2894/tab-article-info
Textquelle: Barbara Konturek, Ludwig Boltzmann Gesellschaft
Bildquelle: (oben) Die Verformung des Zellkerns löst eine Signalkaskade für das Entkommen von Krebszellen aus. Grafik: Wojciech Garncarz (St. Anna Kinderkrebsforschung)
Bildquelle: (unten) Dr. Alexis Lomakin. Foto: St. Anna Kinderkrebsforschung